Autorius:
Frank Hunt
Kūrybos Data:
13 Kovas 2021
Atnaujinimo Data:
1 Liepos Mėn 2024

Turinys
- Žengti
- 1 metodas iš 3: Naudojant pH matuoklį
- 2 metodas iš 3: su lakmuso popieriumi
- 3 metodas iš 3: pH supratimas
Svarbu išmatuoti vandens pH - rūgštingumo ar šarmingumo laipsnį. Vandenį naudoja augalai ir gyvūnai, nuo kurių esame priklausomi, ir mes jį geriame kiekvieną dieną. Vandens pH vertė gali būti galimo užteršimo požymis, todėl vandens pH matavimas gali būti svarbi visuomenės sveikatos apsaugos priemonė.
Žengti
1 metodas iš 3: Naudojant pH matuoklį
 Kalibruokite zondą ir skaitiklį pagal gamyklos instrukcijas. Gali tekti kalibruoti skaitiklį naudojant medžiagą, kurios pH vertė yra žinoma. Skaitiklį galima reguliuoti pagal tą medžiagą. Jei ketinate tirti vandenį ne laboratorijoje, rekomenduojama atlikti šį kalibravimą likus kelioms valandoms iki lauko bandymų.
Kalibruokite zondą ir skaitiklį pagal gamyklos instrukcijas. Gali tekti kalibruoti skaitiklį naudojant medžiagą, kurios pH vertė yra žinoma. Skaitiklį galima reguliuoti pagal tą medžiagą. Jei ketinate tirti vandenį ne laboratorijoje, rekomenduojama atlikti šį kalibravimą likus kelioms valandoms iki lauko bandymų. - Prieš naudojimą zondą nuplaukite švariu vandeniu. Džiovinkite švaria šluoste.
 Paimkite vandens mėginį ir supilkite jį į švarų indą.
Paimkite vandens mėginį ir supilkite jį į švarų indą.- Vanduo turi būti pakankamai gilus, kad panardintų elektrodo galiuką.
- Palikite mėginį kuriam laikui, kad temperatūra stabilizuotųsi.
- Termometru matuojama mėginio temperatūra.
 Sureguliuokite matuoklį pagal mėginio temperatūrą. Zondo jautrumui įtakos turi vandens temperatūra, todėl matavimas gali būti tikslus tik įvedus temperatūros duomenis.
Sureguliuokite matuoklį pagal mėginio temperatūrą. Zondo jautrumui įtakos turi vandens temperatūra, todėl matavimas gali būti tikslus tik įvedus temperatūros duomenis.  Į mėginį įdėkite zondą. Palaukite, kol skaitiklis pasieks pusiausvyrą. Skaitiklis yra pastovios būsenos, kai rodmenys yra stabilūs.
Į mėginį įdėkite zondą. Palaukite, kol skaitiklis pasieks pusiausvyrą. Skaitiklis yra pastovios būsenos, kai rodmenys yra stabilūs.  Perskaitykite mėginio pH matavimą. PH matuoklis duoda rezultatą skalėje 0-14. Jei vanduo yra grynas, vertė yra maždaug 7. Užrašykite išvadas.
Perskaitykite mėginio pH matavimą. PH matuoklis duoda rezultatą skalėje 0-14. Jei vanduo yra grynas, vertė yra maždaug 7. Užrašykite išvadas.
2 metodas iš 3: su lakmuso popieriumi
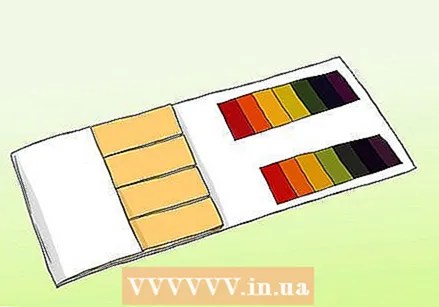 Sužinokite, koks yra pH ir lakmuso popieriaus skirtumas. Norėdami gauti tikslų mėginio nuskaitymą, galite naudoti pH popierių. Tačiau pH popieriaus nereikia painioti su įprastu lakmuso popieriumi. Abi gali būti naudojamos rūgštims ir bazėms tirti, tačiau jos skiriasi svarbiais aspektais.
Sužinokite, koks yra pH ir lakmuso popieriaus skirtumas. Norėdami gauti tikslų mėginio nuskaitymą, galite naudoti pH popierių. Tačiau pH popieriaus nereikia painioti su įprastu lakmuso popieriumi. Abi gali būti naudojamos rūgštims ir bazėms tirti, tačiau jos skiriasi svarbiais aspektais. - pH juostelėse yra keletas indikatorių juostų, kurios, veikiamos tirpalo, keičia spalvą. Rūgščių ir bazių stiprumas kiekvienoje juostoje skiriasi. Po pakeitimo spalvų modelį galima palyginti su rinkinyje pateiktais pavyzdžiais.
- Lakmuso popierius yra popieriaus juosta, kurioje yra rūgšties arba bazės (šarminės). Dažniausiai dryžiai yra raudoni (su rūgštimi, kuri reaguoja su bazėmis) ir mėlyna (su baze, kuri reaguoja su rūgštimis). Raudonos juostelės tampa mėlynos, jei medžiaga yra šarminė, o mėlynos juostelės - raudonos, jei medžiaga yra rūgšti. Lakmuso popieriai gali būti naudojami kaip greitas ir lengvas testas, tačiau pigiausios veislės ne visada tiksliai parodo tirpalo stiprumą.
 Paimkite vandens mėginį ir supilkite jį į švarų indą. Vanduo turi būti pakankamai gilus, kad panardintų juostelę.
Paimkite vandens mėginį ir supilkite jį į švarų indą. Vanduo turi būti pakankamai gilus, kad panardintų juostelę.  Panardinkite bandinio juostelę į mėginį. Pakanka kelių sekundžių ekspozicijos. Po kelių akimirkų popieriaus indikatorių juostos pakeis spalvą.
Panardinkite bandinio juostelę į mėginį. Pakanka kelių sekundžių ekspozicijos. Po kelių akimirkų popieriaus indikatorių juostos pakeis spalvą.  Bandymo juostelės galą palyginkite su spalvų lentele, kuri buvo pridėta prie popieriaus. Kortelės spalva ar spalvos turi sutapti su bandymo juostelės spalva ar spalvomis. Tada spalvų žemėlapis susieja spalvų modelius su pH lygiais.
Bandymo juostelės galą palyginkite su spalvų lentele, kuri buvo pridėta prie popieriaus. Kortelės spalva ar spalvos turi sutapti su bandymo juostelės spalva ar spalvomis. Tada spalvų žemėlapis susieja spalvų modelius su pH lygiais.
3 metodas iš 3: pH supratimas
 Sužinokite, kaip apibrėžiamos rūgštys ir bazės. Rūgštingumą ir šarmingumą (terminas, vartojamas apibūdinant bazes) apibūdina vandenilio jonai, kuriuos jie dovanoja arba pasisavina. Rūgštis yra medžiaga, kuri dovanoja (arba „dovanoja“) vandenilio jonus, o bazė - medžiaga, absorbuojanti papildomus vandenilio jonus.
Sužinokite, kaip apibrėžiamos rūgštys ir bazės. Rūgštingumą ir šarmingumą (terminas, vartojamas apibūdinant bazes) apibūdina vandenilio jonai, kuriuos jie dovanoja arba pasisavina. Rūgštis yra medžiaga, kuri dovanoja (arba „dovanoja“) vandenilio jonus, o bazė - medžiaga, absorbuojanti papildomus vandenilio jonus.  Supraskite pH skalę. PH skaičius naudojamas vandenyje tirpių medžiagų rūgštingumo ar šarmingumo laipsniui matuoti. Vandenyje paprastai yra vienodas hidroksido jonų (OH−) ir hidronio jonų (H3O +) kiekis. Hidroksido ir hidronio jonų santykis keičiasi į vandenį įpylus rūgščios ar šarminės medžiagos.
Supraskite pH skalę. PH skaičius naudojamas vandenyje tirpių medžiagų rūgštingumo ar šarmingumo laipsniui matuoti. Vandenyje paprastai yra vienodas hidroksido jonų (OH−) ir hidronio jonų (H3O +) kiekis. Hidroksido ir hidronio jonų santykis keičiasi į vandenį įpylus rūgščios ar šarminės medžiagos. - Paprastai tai laikoma skale, kuri eina nuo 0 iki 14 (nors medžiagos gali ir nepatekti į šį diapazoną). Neutralių medžiagų balas yra apie 7, rūgščių - mažiau nei 7, šarminių - daugiau nei 7.
- PH skalė yra logaritminė, tai reiškia, kad sveikųjų skaičių skirtumai rodo dešimteriopą rūgštingumo ar šarmingumo skirtumą. Pavyzdžiui, medžiaga, kurios pH yra 2, yra dešimt kartų rūgštesnė už medžiagą, kurios pH yra 3, ir 100 kartų rūgštesnė nei medžiaga, kurios pH yra 4. Skalė veikia vienodai su šarminėmis medžiagomis, su bet kokiomis sveikasis skaičius reiškia dešimteriopą skirtumą.
 Sužinokite, kodėl mes tikriname vandens pH. Gryno vandens pH yra 7, tačiau olandiško vandentiekio vandens pH paprastai yra nuo 7,5 iki 8,3. Labai rūgštus vanduo (žemos pH vertės vanduo) labiau ištirpina nuodingas chemines medžiagas. Tai gali užteršti vandenį ir padaryti jį nesaugų gerti.
Sužinokite, kodėl mes tikriname vandens pH. Gryno vandens pH yra 7, tačiau olandiško vandentiekio vandens pH paprastai yra nuo 7,5 iki 8,3. Labai rūgštus vanduo (žemos pH vertės vanduo) labiau ištirpina nuodingas chemines medžiagas. Tai gali užteršti vandenį ir padaryti jį nesaugų gerti. - Paprastai patartina išbandyti pH vietoje. Jei paimsite vandens mėginį laboratoriniams tyrimams, anglies dioksidas (CO2) iš oro gali ištirpti vandenyje. Ištirpęs anglies dioksidas reaguoja su vandenyje esančiais jonais ir padidina rūgštingumą baziniuose arba neutraliuose tirpaluose. Siekiant išvengti užteršimo anglies dvideginiu, vandenį reikia ištirti per dvi valandas po surinkimo.