Autorius:
Lewis Jackson
Kūrybos Data:
5 Gegužė 2021
Atnaujinimo Data:
1 Liepos Mėn 2024

Turinys
Mol yra standartinis chemijos matavimo vienetas, naudojamas pažvelgti į skirtingus junginio elementus. Paprastai junginio masė apskaičiuojama gramais (g) ir ją reikia konvertuoti į molinius vienetus. Perėjimas yra gana paprastas, tačiau vis dar yra keletas svarbių žingsnių, kuriuos turime atlikti. Naudodami toliau pateiktą metodą, galite lengvai konvertuoti gramus į apgamus.
Žingsniai
1 dalis iš 2: Apskaičiuokite molekulinę masę
Paruoškite reikiamus reikmenis matematikos uždaviniui išspręsti. Kai turėsite visus turimus įrankius, bus lengviau išspręsti problemą. Ko jums reikia:
- Pieštukas ir popierius. Matematika tampa lengvesnė, kai viską užrašai ant popieriaus. Norėdami pasiekti maksimalų balą, turite pateikti visus veiksmus.
- Periodinė cheminių elementų lentelė: naudojama elementų masės atomams nustatyti.
- Kišeninė skaičiuoklė: naudojama sudėtingiems skaičiams apskaičiuoti.

Nustatykite, kurie elementai yra junginyje, kurį reikia konvertuoti į molinius vienetus. Pirmasis žingsnis apskaičiuojant molekulinę masę yra nustatyti elementus, kurie sudaro junginį. Tai lengva, nes elementų santrumpa yra tik vienas – du simboliai.- Jei medžiaga sutrumpinta dviem raidėmis, pirmoji raidė bus rašoma didžiosiomis raidėmis, o antroji - mažosiomis raidėmis. Pavyzdys: Mg yra magnio elemento santrumpa.
- NaHCO junginiai3 susideda iš keturių elementų: natrio (Na), vandenilio (H), anglies (C) ir deguonies (O).
Nustatykite kiekvieno junginio elemento atomų skaičių. Norėdami apskaičiuoti to junginio masės molekulę, turite žinoti kiekvienos junginio medžiagos atominį skaičių. Mažas skaičius šalia elemento inicialų žymi elemento atominį skaičių.- Pavyzdys: junginys H2O turi du vandenilio atomus ir vieną deguonies atomą.
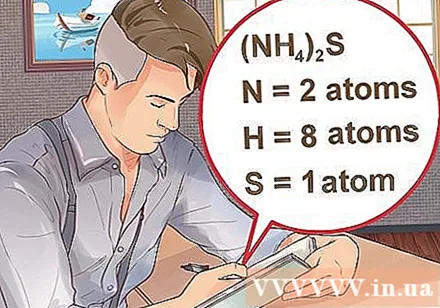
- Jei skliausteliuose rašomas junginys, po kurio yra nedidelis indeksas, tai reiškia, kad kiekvienas skliaustuose esantis ingredientas padaugina indeksą. Pavyzdys: junginys (NH4)2S susideda iš dviejų N atomų, aštuonių H atomų ir vieno S atomo.

Užrašykite kiekvieno elemento kubinį atominį popierių. Periodinės lentelės naudojimas yra lengviausias būdas surasti elemento kubinį atomą. Suradę elementą periodinėje lentelėje, pamatysite atominę masę tiesiai po elemento piktograma.- Pavyzdžiui, kubinis deguonies atomas yra 15,99.
Apskaičiuokite molekulinę masę. Medžiagos masės molekulė lygi kiekvieno elemento atomų skaičiui, padaugintam iš to elemento masės atomo. Šis kiekis yra būtinas perskaičiuojant gramais į molius.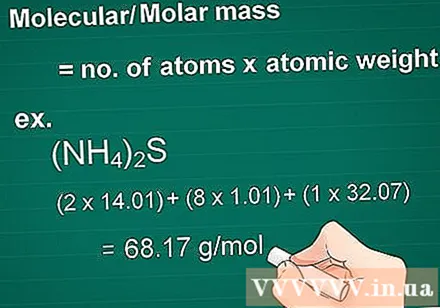
- Pirmiausia kiekvieno junginio elemento atominį skaičių padauginkite iš jo masės atomo.
- Tada kartu suberkite junginio elementų mases.
- Pavyzdys: Junginio molekulinė masė (NH4)2S = (2 x 14,01) + (8 x 1,01) + (1 x 32,07) = 68,17 g / mol.
- Molekulinė masė taip pat žinoma kaip molinė masė.
2 dalis iš 2: Konvertuokite gramus į mol
Nustatykite konversijos formulę. Norėdami sužinoti junginio molių skaičių, padalykite junginio gramų skaičių iš to junginio molinės masės.
- Formulė: molių skaičius = masė (gramais) / molinė junginio masė (gramais / mol)
Įdėkite skaičius į formulę. Nustačius tinkamą formulę, kitas žingsnis yra apskaičiuotų skaičių pakeitimas į formulę. Jei norite įsitikinti, kad duomenys yra teisingoje padėtyje, galite juos patikrinti nuslopindami įrenginį. Jei po paprastumo likęs vienetas yra apgamai, tada jūs nustatote teisingai.
Išspręskite lygtį. Skaičiuokliu padalykite masę iš kubinės medžiagos ar junginio molekulės. Dalmuo bus ieškomos medžiagos ar junginio molių skaičius.
- Pavyzdžiui, problema yra dėl 2 g vandens (H2O) ir paprašykite jį konvertuoti į molinius vienetus. Turime H molinę masę2O yra 18 g / mol. Padalinkite 2 iš 18, taigi turite 0,1111 mol H2O.
Patarimas
- Nepamirškite į atsakymus įtraukti elemento ar junginio pavadinimą.
- Jei jūsų prašoma pateikti pratimą ar viktoriną, įsitikinkite, kad aiškiai parodėte savo atsakymus, sukdami ratus ar nupiešdami langelį aplink atsakymus.
Ko tau reikia
- Cheminė periodinė lentelė
- Pieštukas
- Popierius
- Kompiuteris
- Chemijos problemos