Autorius:
Lewis Jackson
Kūrybos Data:
12 Gegužė 2021
Atnaujinimo Data:
1 Liepos Mėn 2024

Turinys
Nustatyti neutronų skaičių atome yra gana paprasta, jums net nereikia atlikti jokių eksperimentų. Norėdami apskaičiuoti neutronų skaičių įprastame atome ar izotope, jums tiesiog reikia paruošti periodinę lentelę ir laikytis instrukcijų.
Žingsniai
1 metodas iš 2: raskite neutronų skaičių normaliame atome
Nustatykite elemento padėtį periodinėje lentelėje. Pavyzdžiui, elementą osmium (Os) rasime šeštoje eilėje nuo viršaus.
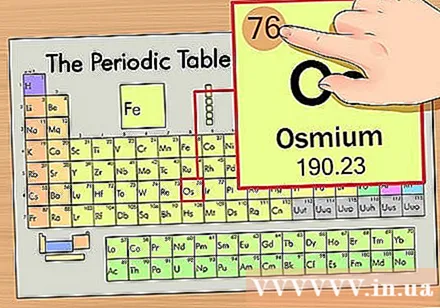
Raskite elemento atominį skaičių. Tai labiausiai pastebimas skaičius, einantis pro kiekvieną elementą ir esantis virš pirminio simbolio (lentoje, kurią naudojame, kitų skaičių nėra). Atomo skaičius yra protonų skaičius viename to elemento atome. Os yra skaičius 76, o tai reiškia, kad osmio atome yra 76 protonai.- Protonų skaičius elemente niekada nesikeičia; iš esmės tai yra apibrėžianti elemento charakteristika.
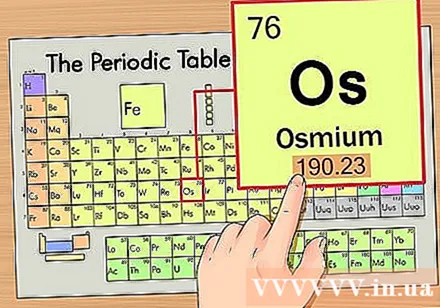
Raskite elemento atominę masę. Šis skaičius paprastai yra po pagrindiniu simboliu. Atkreipkite dėmesį, kad šio pavyzdžio periodinėje lentelėje yra tik atominis skaičius ir jokio atominio svorio. Ne visos periodinės lentelės. Osmio atominė masė yra 190,23.
Apgaubkite atominę masę iki artimiausio sveikojo skaičiaus, kad gautumėte atominę masę. Pavyzdžiui, 190,23 būtų suapvalinta iki 190, taigi osmio atominė masė yra 190.- Atomo svoris yra vidutinė to paties cheminio elemento izotopų vertė, todėl paprastai tai nėra sveikasis skaičius.
Iš atomo masės atimkite atominį skaičių. Kadangi didžioji atominės masės dalis yra protonų ir neutronų masė, atimdami protonų skaičių iš atominės masės (t. Y. Atominio skaičiaus), gausite suskaičiuoti gaukite neutronų skaičių atome. Skaičius po dešimtainio taško reiškia labai mažą elektronų masę atome. Šiame pavyzdyje turime: 190 (masės atomas) - 76 (protonų skaičius) = 114 (neutronų skaičius).
Įsiminkite receptą. Norėdami sužinoti neutronų skaičių, paprasčiausiai taikome šią formulę: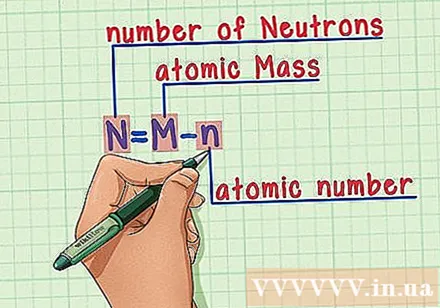
- N = M - n
- N = neutronų skaičius
- M = atominė masė
- n = atominis skaičius
- N = M - n
2 metodas iš 2: raskite neutronų skaičių izotope
Nustatykite elemento padėtį periodinėje lentelėje. Kaip pavyzdį paimkime anglies-14 izotopą. Kadangi anglies-14 izotopo forma yra tiesiog anglis (C), anglies ieškokite periodinėje lentelėje (antra eilutė iš viršaus).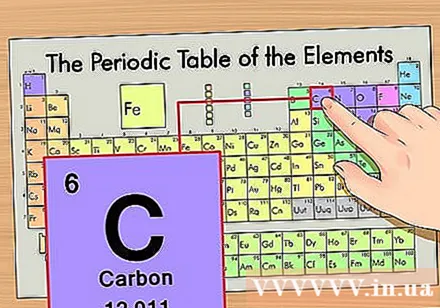
Raskite elemento atominį skaičių. Tai labiausiai pastebimas skaičius, einantis pro kiekvieną elementą ir esantis virš pirminio simbolio (lentoje, kurią naudojame, kitų skaičių nėra). Atomo skaičius yra protonų skaičius viename to elemento atome. C yra skaičius 6, o tai reiškia, kad anglies atome yra 6 protonai.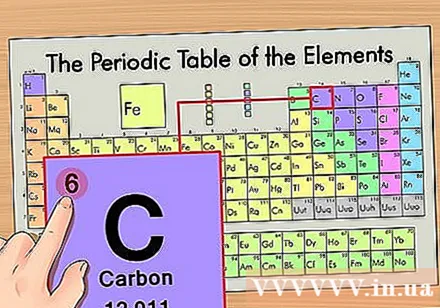
Raskite atominę masę. Su izotopais tai padaryti yra labai lengva, nes jie pavadinti pagal atominę masę. Pavyzdžiui, anglies-14 atominė masė būtų 14. Suradę izotopo atominę masę, likusieji neutronų skaičiaus nustatymo veiksmai bus tokie patys kaip įprasto atomo.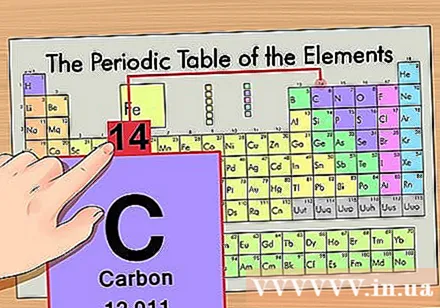
Iš atomo masės atimkite atominį skaičių. Kadangi didžioji atominės masės dalis yra protonų ir neutronų masė, atimdami protonų skaičių iš atominės masės (t. Y. Atominio skaičiaus), gausite suskaičiuoti gaukite neutronų skaičių atome. Skaičius po dešimtainio taško reiškia labai mažą elektronų masę atome. Šiame pavyzdyje turime: 14 (masės atomas) - 6 (protonų skaičius) = 8 (neutronų skaičius).
Įsiminkite receptą. Norėdami sužinoti neutronų skaičių, mes naudojame šią formulę: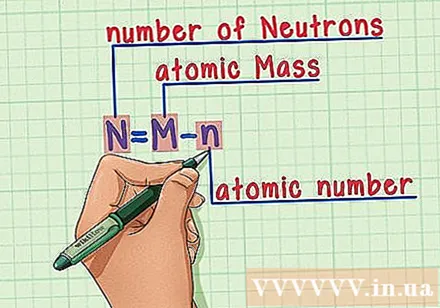
- N = M - n
- N = neutronų skaičius
- M = atominė masė
- n = atominis skaičius
- N = M - n
Patarimas
- Elemento masė daugiausia yra protonų ir neutronų masė, o elektronų ir kitų elementų masė yra nereikšminga (arti nulio). Kadangi protono masė yra maždaug lygi neutrono masei, o atominis skaičius reiškia protonų skaičių, mums reikia tik atimti protonų skaičių iš bendros masės.
- Jei neprisimenate periodinėje lentelėje esančių skaičių reikšmės, nepamirškite, kad periodinė lentelė paprastai kuriama remiantis atominiais skaičiais (t. Y. Protonų skaičiumi), pradedant nuo 1 (vandenilis) ir didinant vieną vienetą nuo iš kairės į dešinę, baigiantis 118 (ununoctium). Kadangi protonų skaičius yra kiekvieno atomo atpažinimo bruožas, tai yra paprasčiausia savybė, ant kurios išdėstyti elementai. (Pavyzdžiui, atomas su 2 protonais visada yra helis, kaip ir atomas, turintis 79 protonus, visada yra auksas.)
Šaltiniai ir citatos
- Interaktyvi periodinė lentelė